造血细胞克隆的扩增,携带血液恶性肿瘤中常见突变基因的变异,但在缺乏造血细胞计数改变或其他明确定义的疾病标准的情况下,被称为克隆性造血(CH)。CH常见于老年个体,并与多种有害健康影响相关。这些影响高度依赖于突变的类型及其显现的细胞环境。造血干细胞和祖细胞(HSPC)区室以及自我更新的较成熟细胞中的突变与恶性疾病风险增加相关;而通过造血作用渗入非自我更新的成熟细胞中的突变则与免疫功能改变及随之而来的全身效应相关,这可能引发或加剧多种非恶性疾病。瑞士苏黎世大学Francisco Caiado教授与Markus G. Manz教授共同回顾了CH的定义、主要遗传驱动因素和谱系外显度,并重点阐述CH如何影响血液系统和非血液系统疾病。
01
引言
造血系统通过持续产生成熟血-免疫细胞维持机体关键功能。其层级结构由稀有的造血干细胞(HSCs)维持,HSC分化为高度增殖的造血祖细胞(HPC),最终生成成熟血细胞。HSC定位于骨髓微环境,通过自我更新维持细胞池规模,同时产生HPC并逐步分化为效应细胞。
正常造血中,HSC池呈高度多克隆性,65岁以下人群约2万至20万HSC参与白细胞生成。而75岁以上人群造血克隆多样性显著下降,30%~60%的造血功能由12~18个独立HSC克隆主导。这一现象源于年龄相关的HSC功能衰退及携带驱动突变的HSC克隆选择性扩张。此类克隆动态演变导致克隆性造血(CH,又称年龄相关克隆性造血)的频发,并与恶性进展(髓系及淋系肿瘤)及非造血系统功能障碍(心血管、肺、肾、肝、风湿性疾病)风险增加相关,提示CH不仅具有前白血病特征,还可能广泛影响血-免疫系统功能。本文系统阐述CH的核心特征,重点分析其对血液及非血液系统肿瘤发生的影响、与非恶性疾病的关联及免疫治疗意义。
02
克隆性造血(CH):定义、发生率与驱动因素
根据世界卫生组织(WHO)分类,CH指存在来源于突变造血多能干细胞/祖细胞的细胞群体,其携带选择性生长优势,但无不明原因细胞减少、血液肿瘤或其他克隆性疾病特征。CH包含复杂实体,定义依据驱动基因身份、等位基因频率(VAF)、突变基因类型及是否存在染色体镶嵌变异(mCA)。
本文聚焦最常见形式——潜在不确定意义的克隆性造血(CHIP),其定义为血液或骨髓细胞中检测到已知髓系白血病驱动基因(VAF≥2%或男性X连锁基因突变VAF≥4%),且无明确血液疾病诊断标准或不明原因细胞减少。成人(40-70岁)CHIP发生率约5%,70岁以上人群升至10%~20%。约90% CHIP携带单突变,以表观遗传调控基因DNMT3A、TET2、ASXL1(DTA)为主,占复发突变的三分之二,其余包括JAK2、TP53、GNAS、PPM1D、BCORL1、SF3B1等髓系肿瘤驱动基因。值得注意的是,CHIP发生率、克隆大小及复杂性(多突变)均随年龄增长而升高。
需区分的是,携带持续不明原因细胞减少的CHIP被WHO定义为潜在不确定意义的克隆性细胞减少(CCUS),其突变谱与CHIP重叠但发生率更低、克隆更大更复杂,且进展为髓系肿瘤(MN,包括急性髓系白血病、骨髓增生异常综合征及髓系增殖性肿瘤)风险更高。本文以CH为统称涵盖CHIP与CCUS,因部分研究未明确区分二者。
 年龄与克隆性造血的关键特征密切相关
年龄与克隆性造血的关键特征密切相关
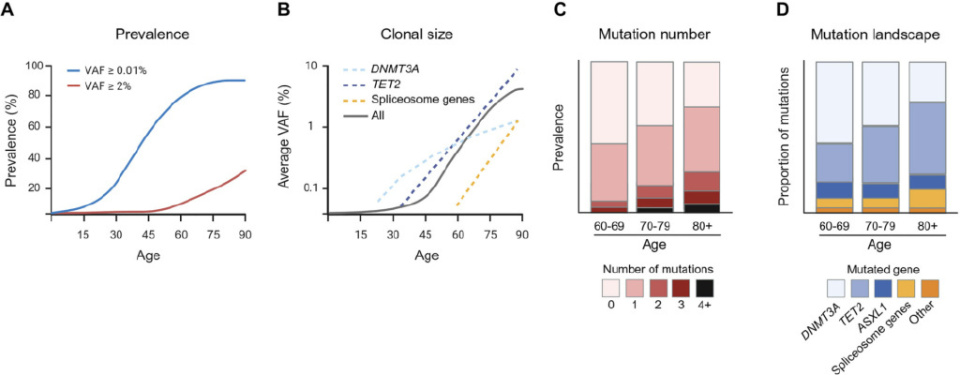
(A)CH的估计患病率随年龄增长而上升,具体数值取决于作为CH定义阈值的突变等位基因频率(VAF),而VAF的选取又与所采用的测序方法有关。
(B)示意图显示平均克隆大小随年龄的变化(灰色实线),提示高龄阶段克隆体积显著增大。不同突变类型的克隆扩增轨迹以虚线表示:DNMT3A突变克隆在较早阶段即呈现较高的扩增速率;TET2突变克隆起始较晚,随后终生以相对恒定的速率扩增;剪接体基因突变克隆(包括SF3B1、SRSF2和U2AF1)起病最晚,但扩增速率最高。
(C)示意图按年龄组展示每个个体的突变数目分布,表明高龄个体的突变数目显著增加
(D)示意图按年龄组展示各驱动基因突变在所有检出突变中的占比,提示随着年龄增长,DNMT3A突变的相对频率下降,而TET2和ASXL1突变的相对频率上升;剪接体突变类别同样包括SF3B1、SRSF2和U2AF1。
03
CHIP的谱系特异性突变特征
CHIP最初主要被视为髓系克隆性造血形式。这归因于:根据定义,最初在CHIP携带者中寻找和识别的突变通常见于髓系恶性肿瘤;以及后续研究证实,大多数CHIP携带者罹患髓系(而非淋系)肿瘤的风险增加。与此一致的是,研究显示CHIP携带者成熟造血细胞群中的突变VAF在单核细胞、粒细胞和自然杀伤细胞(NK细胞)中高于B细胞或T细胞。
此外,在骨髓样本中,CHIP突变可见于Lin−CD34+CD38− HSPCs(造血干/祖细胞),随后扩增至髓系定向祖细胞,强烈提示CHIP起源于突变的HSPCs,并优先向髓系分支扩增,而在淋系区室的外显度和/或扩增程度较低。这可能源于某些CHIP突变对B细胞和T细胞发育复杂过程的适应性降低,以及成年期整体B细胞和T细胞生成减少(其稳态部分由成熟的B细胞和T细胞驱动)。值得注意的是,近期也有研究提出CH可作为淋系统恶性肿瘤的前驱病变。此类实体发生率远低于髓系CHIP,将在文末简要讨论。
04
CH与血液系统肿瘤进展
CH被视为造血系统的前恶性状态,因其携带的体细胞突变常为血液肿瘤的创始突变。CHIP与CCUS均与MN风险增加相关(约10-12倍,CCUS风险略高),年转化率0.5%~1%。
风险高度依赖以下因素:
(1)突变基因:DNMT3A单突变风险最低,剪接因子基因(SF3B1、SRSF2)、TP53、IDH1/2、RUNX1突变风险最高;
(2)克隆内突变数量:多突变(2个)风险更高;
(3)克隆大小:VAF≥20%风险更高;
(4)红细胞特征:红细胞分布宽度(RDW)≥15%及平均红细胞体积(MCV)≥100fL提示风险升高;
(5)细胞减少:CCUS风险高于CHIP;
(6)年龄:65岁以上人群风险更高。
近期研究进一步强调,CHIP携带者中的突变特征与罹患特定髓系肿瘤的倾向性增加相关。具体而言,SF3B1与SRSF2/TET2共突变病例与MDS高风险相关;SRSF2/IDH2共突变病例更易进展为AML;而DNMT3A-R882突变则与AML特异性相关。总之,结合不同CH参数建立髓系肿瘤转化风险评分的工作对于理解癌前病变进展至完全恶性状态背后的生物学机制至关重要,并有助于实现更精确的CH携带者分层和临床管理。
05
CHIP与非恶性疾病
 CHIP对健康的影响示意图
CHIP对健康的影响示意图
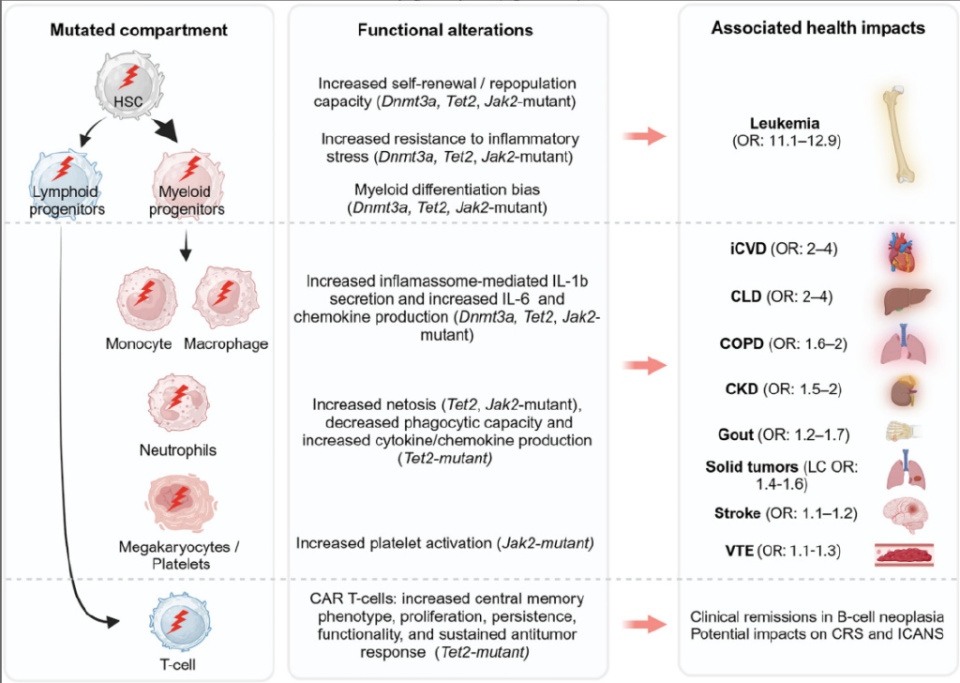
左侧展示受CHIP相关突变影响的细胞(造血干/祖细胞,HSC);中间列举与细胞类型特异性CHIP突变相关的功能性细胞改变;右侧总结CHIP已报道影响。中间与右侧之间的红色箭头仅表示关联,并不等同于因果。
越来越多的证据表明,成熟造血区室中的CHIP突变特异性效应可导致免疫细胞功能障碍,并增加非恶性疾病风险和总体死亡率。实际上,多种年龄相关炎症性疾病与CHIP呈正相关,并可能作为疾病修饰因子。这些疾病包括心血管疾病、慢性肝病、慢性肾病(CKD)、慢性阻塞性肺病(COPD)、痛风、骨质疏松、脑卒中以及静脉血栓栓塞(VTE)。值得注意的是,迄今为止CHIP仅被发现对阿尔茨海默病具有保护作用,但潜在机制仍不清楚。
除白血病转化外,缺血性心血管疾病(iCVD)是CHIP携带者中风险最高的病理状态。与无突变者相比,CHIP携带者罹患冠心病的风险增加约2倍,心肌梗死风险增加约4倍,其中TET2和JAK2突变病例关联最强。重要的是,与进展为髓系恶性肿瘤风险相似,克隆大小同样对iCVD结局具有预后意义:VAF ≥ 10%的个体较小克隆者具有更高的iCVD风险。机制上,小鼠模型研究将这一效应归因于Dnmt3a/Tet2突变髓系细胞(尤其是在动脉粥样硬化斑块形成背景下)产生促炎细胞因子(IL-1β、IL-6及趋化因子)增加。与此一致,抗IL-1β药物卡那单抗(Canakinumab)抗炎溶栓结局研究(CANTOS)的探索性分析显示,受试者的心血管事件减少,尤其见于TET2突变CHIP携带者。
肝病也显著受CHIP影响:VAF ≥ 10%使CHIP携带者罹患慢性肝病(CLD)、非酒精性肝脂肪变性和肝硬化的风险加倍。该关联也高度依赖CHIP突变类型:JAK2突变CHIP的CLD风险增加17.6倍,TET2突变CH增加5.4倍,而DNMT3A突变风险较低。Tet2突变CHIP小鼠模型研究进一步提示,肝内驻留巨噬细胞来源的炎症小体依赖性炎症反应(IL-6、CXCL1、CCL22、CCL17)参与了这一结局。
CHIP对慢性肾病(CKD)、慢性阻塞性肺病(COPD)、痛风、骨质疏松、脑卒中和静脉血栓栓塞(VTE)发生率的影响较温和。在CKD中,CHIP导致5年随访期间肾衰竭风险增加2.2倍,且CKD相关并发症(包括贫血背景下的肾病)风险增加。在COPD中,携带CHIP者中-重度、重度或极重度COPD风险分别为非携带者的1.6倍和2.2倍。合并COPD的Tet2突变CHIP小鼠模型进一步发现,造血细胞中Tet2缺失会增强肺部炎症,增加IFN信号传导,降低TGF-β信号传导,并加速肺气肿发展。在痛风病例中,经校正常见风险因素后,VAF ≥ 10%的CHIP患者事件风险是未患CHIP者的1.3倍;TET2突变CHIP风险尤其更高。体内机制研究表明,Tet2基因敲除小鼠中,由于巨噬细胞产生更多IL-1β,单钠尿酸盐诱导的炎症以NLRP炎症小体依赖性方式加重。在骨质疏松方面,CHIP患者事件风险是非CHIP患者的1.4倍。更大的克隆(尤其DNMT3A突变且VAF ≥ 10%)与较低的骨密度显著相关,符合加速骨质流失的特征。机制上,该过程与促炎因子相关,包括Dnmt3a突变巨噬细胞中Irf3-NF-κB介导的IL-20表达增加。总体而言,CHIP相关且年龄相关的炎性疾病符合小鼠研究结果,特别是Tet2和Dnmt3a突变区室增强了炎症反应。
06
CHIP与实体瘤
CHIP与实体瘤的关联最初见于接受治疗的实体瘤患者队列。一项纳入8810例患者的MSKCC研究显示,25%患者存在CHIP,且VAF>10%者总生存期缩短,主要死因为原发肿瘤进展。后续研究部分证实该关联,但治疗相关因素(如化疗诱导DNA损伤反应基因突变)及共病(年龄、吸烟)可能混淆因果。大型非癌症队列研究降低了混杂因素:UK Biobank的200,453例分析显示,CHIP(尤其VAF>10%)与肺癌、肾癌、淋巴瘤及肉瘤相关,DNMT3A突变CHIP还与胃癌、膀胱癌相关,剪接因子SF3B1/SRSF2突变与结直肠癌、头颈癌相关;628,388例个体分析显示CHIP与肺癌、皮肤癌、前列腺癌及乳腺癌相关。
肺癌是CHIP影响最显著的实体瘤类型,多个队列显示CHIP(尤其DNMT3A、TET2、ASXL1突变且VAF>10%)使肺癌风险增加36%。机制上,突变免疫细胞可能直接参与肿瘤微环境(TME)功能异常,人类实体瘤样本中已检测到突变免疫细胞。小鼠模型显示,Tet2缺失的造血细胞通过IL-6介导的免疫抑制促进肝癌及乳腺癌生长,或通过S100a8/S100a9上调增强癌细胞VEGF-A分泌,增加肺癌血管生成及生长。但Tet2突变在黑色素瘤中显示相反作用,通过诱导促炎巨噬细胞表型促进T细胞浸润,减少肿瘤负荷。不同CHIP驱动基因对肿瘤生物学的具体影响需进一步研究(如Dnmt3a、Asxl1、p53突变)。
07
CHIP与免疫治疗/血液肿瘤治疗
造血干细胞移植(HSCT)包括自体(auto-HSCT)及异基因(allo-HSCT)移植。auto-HSCT多用于化疗后造血衰竭的过渡,allo-HSCT则用于治疗先天性或获得性骨髓衰竭及利用供体细胞的移植物抗肿瘤效应。CHIP常见于HSCT患者:auto-HSCT后CHIP发生率10%~30%(老年患者更高),以DNA损伤反应基因(TP53、PPM1D)突变为主,可能与化疗前暴露选择耐药突变及移植后造血微环境减少的增殖优势相关。auto-HSCT前CHIP与治疗相关髓系肿瘤(t-MN)风险增加及总生存期缩短相关。
allo-HSCT供体CHIP发生率16%~24%,突变谱与普通人群重叠,供体突变常转移至受体并轻度扩张。移植后克隆选择模式包括“剪枝选择”(供体预存克隆主导)和“生长选择”(多突变克隆在受体中扩张)。供体来源白血病罕见,多见于TP53/剪接因子突变或DDX41胚系突变供体。供体CHIP不影响受体总生存期、无进展生存期或非复发死亡率,但DNMT3A突变CHIP(VAF>1%)通过增加IL-12介导的炎症环境降低复发风险,同时增加慢性移植物抗宿主病风险,改善受体生存。
CAR-T细胞治疗中,TET2、DNMT3A、CBL等CHIP相关基因突变可增强CAR-T细胞中央记忆表型,促进增殖、持久性及抗肿瘤功能,与临床缓解相关。但CHIP对接受CAR-T治疗的癌症患者影响复杂,研究显示无显著影响、年轻患者完全缓解率及细胞因子释放综合征(CRS)严重度增加,或增加神经毒性、CRS严重度及治疗相关髓系肿瘤风险,需进一步机制研究指导干预策略。
08
淋系克隆性造血与淋系肿瘤
CH最初通过检测髓系肿瘤驱动基因定义,近期研究聚焦淋系肿瘤驱动基因及染色体镶嵌变异,将CH分为髓系CHIP(M-CHIP)、淋系CHIP(L-CHIP)、髓系mCA(M-mCA)及淋系mCA(L-mCA)。L-CHIP定义为血液白细胞中淋系肿瘤驱动基因VAF≥2%且无淋系肿瘤诊断。其发生率随年龄增长,但低于M-CHIP(40-70岁成人约1%,老年人群低一个数量级)。L-CHIP突变谱以淋系肿瘤相关基因为主,无明确优势突变。L-CHIP与淋系肿瘤(如慢性淋巴细胞白血病、小淋巴细胞淋巴瘤)风险增加相关,但无M-CHIP相关的心血管疾病或全因死亡风险。
L-CHIP的克隆起源可能涉及HSC及淋系祖细胞,但需进一步证实。需注意,成熟T/B细胞因抗原受体重排及程序性突变(B细胞)可能形成低水平克隆,需与L-CHIP区分(如低计数单克隆B淋巴增多症或T细胞克隆不确定意义)。L-CHIP向恶性转变的风险因素(如克隆大小、多突变)仍待明确,但淋巴细胞增多可能提示风险升高。
 造血系统克隆性疾病中的起源细胞及其意义示意图
造血系统克隆性疾病中的起源细胞及其意义示意图
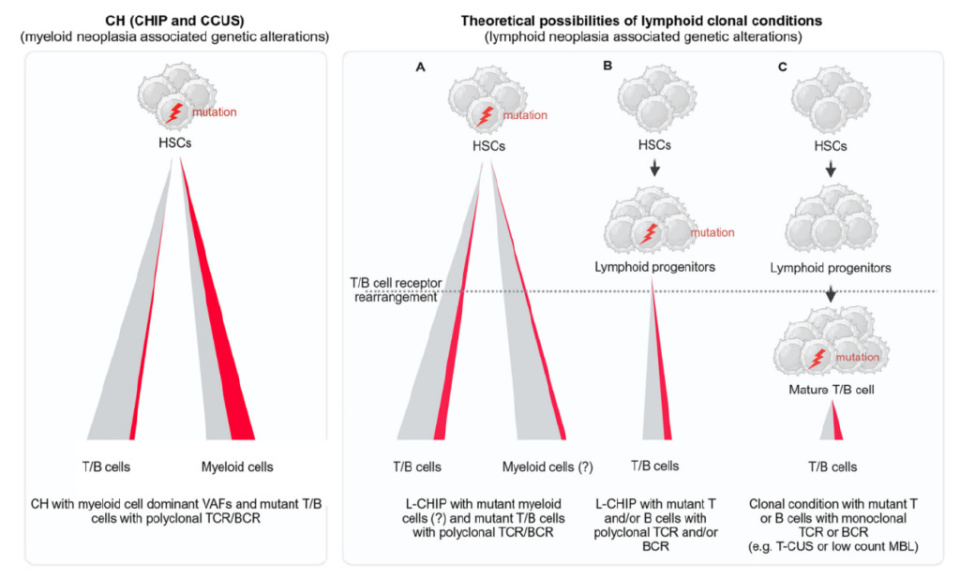
在造血系统克隆性疾病中,起源细胞的定位决定了突变分布模式与疾病特征。以克隆性造血(包含CHIP与CCUS)为例(左图示),突变通常发生于造血干细胞(HSC)层面,导致成熟髓系细胞区室呈现高变异等位基因频率(VAF),而淋系区室突变检出率显著较低。
与之相对,淋系克隆性疾病(右图示)存在三种起源场景:
情形A中,HSC发生的突变可传递至淋系(推测亦可能影响髓系)子代细胞;淋系祖细胞经历抗原受体重排后,形成T/B细胞受体多样化的突变克隆,但此类L-CHIP突变如何向髓系谱系传递尚不明确(图示以问号标注)。
情形B指突变发生于受体重排前的淋系祖细胞,最终形成受体多样化的突变克隆。
情形C则源于已完成T/B细胞受体重排的淋巴细胞发育阶段,其克隆性扩增形成单克隆性T/B细胞受体突变群体,此类克隆可见于单克隆B淋巴细胞增多症(MBL)或意义未明T细胞克隆(T-CUS)。
为简化示意,其他谱系(如自然杀伤细胞)的突变分布未予展示。