近日,EHA 2025大会报告(EHA Perspectives Congress Reports)正式发布,分为恶性血液学和非恶性血液学两大部分。报告全面梳理了大会期间公布的重大科研成果与临床进展,为全球血液学专业人士提供了深入了解领域前沿动态的权威参考。本期特整理非恶性血液学报告中关于“造血干细胞及其微环境:从生理到病理”的专题内容,分为上下两部分,旨在为大家提供富有价值的临床与科研洞见。
精选演讲概览
造血干细胞(HSCs)位于造血细胞层级的顶端,在血液细胞的持续更新中起着至关重要的作用。造血干细胞的特点是具备自我更新和分化为多种细胞类型的潜能,能够在骨髓(BM)中产生所有成熟的血细胞谱系。其通过一系列中间前体细胞发挥作用,为每个谱系提供独立的更新途径。而骨髓微环境(或微环境)则通过提供造血干细胞自我更新和持续造血所需的必需成分来调控其维持和分化。
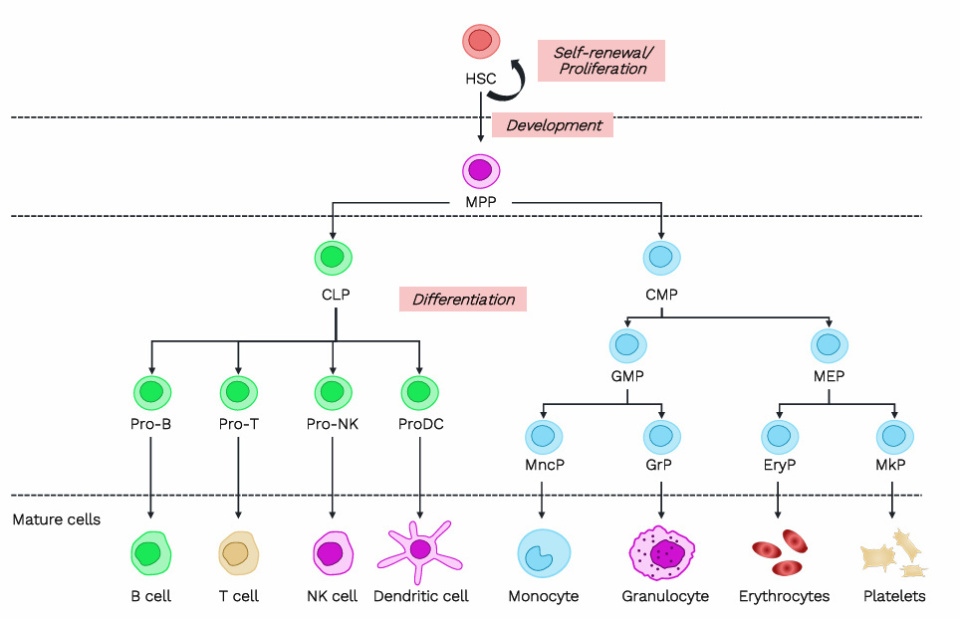 正常造血各阶段概述
正常造血各阶段概述
命运追踪以识别谱系限制的HSC途径
除了此前已鉴定出的髓系偏向和淋巴系偏向的造血干细胞(HSC)外,其他谱系偏向性限制的造血干细胞的完整范围及其相互作用仍有待阐明。
通过单细胞移植研究,发现小鼠造血干细胞具有有限的谱系限制模式,其中仅发现了血小板限制性(P限制性)造血干细胞[1]。另一方面,在幼鼠中血小板-红系髓系(PEM)和PEM+B 细胞(PEMB)限制性谱系的造血干细胞较为常见。研究中未观察到其他类型的谱系限制或偏向性模式。
血管性血友病因子(Vwf)阳性的P-HSCs和Vwf阴性的多谱系造血干细胞(多HSCs)之间并不存在层级关系,它们分别采用不同的前体途径来补充血小板,并补充表型和分子特征均不同的巨核细胞前体。在急性前体细胞耗竭(如化疗)和衰老过程中,经由P限制路径的血小板生成会短暂增强。
在人类造血干细胞中,研究人员采用克隆性造血(CH)驱动突变进行克隆性造血干细胞谱系命运追踪。结果显示,PEM和PEMB限制性造血干细胞是唯一观察到的谱系限制性造血干细胞。PEM限制性和PEMB限制性造血干细胞由多谱系PEMB和T细胞(PEMBT)造血干细胞层级补充。PEM限制性和PEMBT限制性造血干细胞会随着衰老而扩增,但在年轻时就已出现。
回顾性和前瞻性分析表明,人类造血干细胞的克隆性谱系补充模式随着时间推移及移植后保持稳定,提示这些模式是内在编程的。
长期造血干细胞(LT-HSCs)的标记物
长期造血干细胞(LT-HSCs)通过自我更新维持终身造血,同时保持干细胞库。经典的造血干细胞标记物,如CD49f(整合素α6)和CD90,通常用于在人类中区分短期造血干细胞(ST-HSC)和长期造血干细胞(LT-HSC)。然而,能够精确区分长期造血干细胞与短期前体细胞(这些前体细胞在生命过程中具有短暂的再造血能力)的免疫表型标记物仍然有限。
ATP2B1(钙离子转运ATP酶)是一种新发现的细胞表面标记物,可在从胎肝、新生儿脐血到成人动员外周血等不同发育阶段来源的CD49f+LT-HSC中呈异质性表达[2]。ATP2B1的表达将当前金标准纯化方法获得的CD49f+HSC进一步细分为两个亚群:其中 CD49f+ATP2B1+ LT-HSC 在体内显示出优于 CD49f+ATP2B1+LT-HSC 的长期重建及自我更新能力。
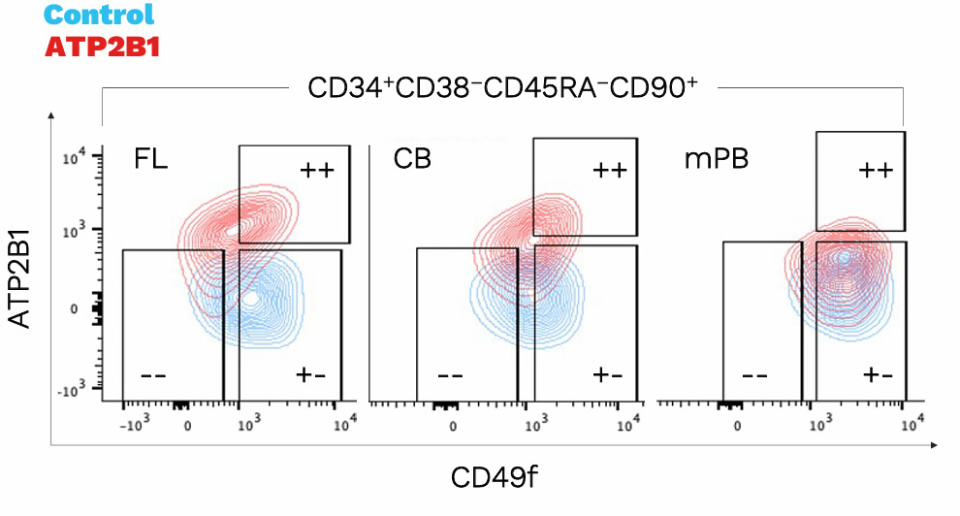 人类造血干细胞中ATP2B1+/–和CD49f+/–细胞的代表性流式细胞术图谱,分别来自胎肝(FL)、新生儿脐血(CB)和动员外周血(mPB)
人类造血干细胞中ATP2B1+/–和CD49f+/–细胞的代表性流式细胞术图谱,分别来自胎肝(FL)、新生儿脐血(CB)和动员外周血(mPB)
精确表位编辑在造血干细胞中的应用
在造血干细胞移植(HSCT)前,通常需要进行骨髓预处理(BM conditioning);然而,传统方法具有较强的基因毒性。使用靶向免疫疗法的非基因毒性骨髓预处理有可能在移植患者中最小化不良事件的发生。
表位编辑是一种精确的基因操作技术,通过引入单核苷酸突变,使造血干细胞和祖细胞(HSPCs)对免疫疗法“隐形”。该方法可在不敲除基因的情况下移除靶表位,从而实现非基因毒性预处理及对HSPCs的体内选择性扩增。
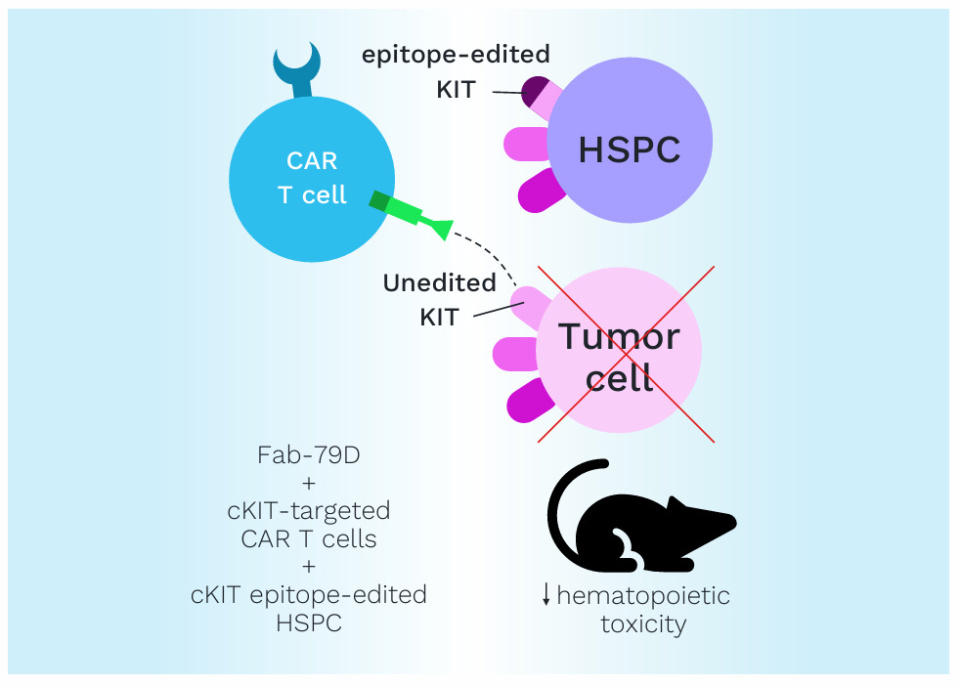
干细胞抗原cKIT/CD117的表位图谱分析显示,KIT H378R突变能够阻断治疗性抗体Fab-79D的结合[3]。验证结果表明,采用腺嘌呤碱基编辑技术安装的KIT H378R仍保留配体结合与胞内信号传导功能[1]。
体内实验表明,通过Fab-79D筛选的KIT表位编辑造血系统,可完整保留HSPC的重建及多系分化能力。表位编辑还可与BCL11A治疗性基因组编辑相结合,实现多重基因工程细胞的体内共选,并诱导胎儿血红蛋白(HbF)表达。
针对不同临床适应证对抗体药效强度的需求差异,研究进一步验证了抗KIT的SR-1克隆——一种SCF阻断单抗,其效力为FAD-79D的25倍。在经过Prime编辑后,该抗体同样可实现非基因毒性的造血系统替代预处理。
表位编辑可能消除与单克隆抗体药代动力学相关的局限性,为创新的造血干细胞移植策略提供支持。
参考文献:
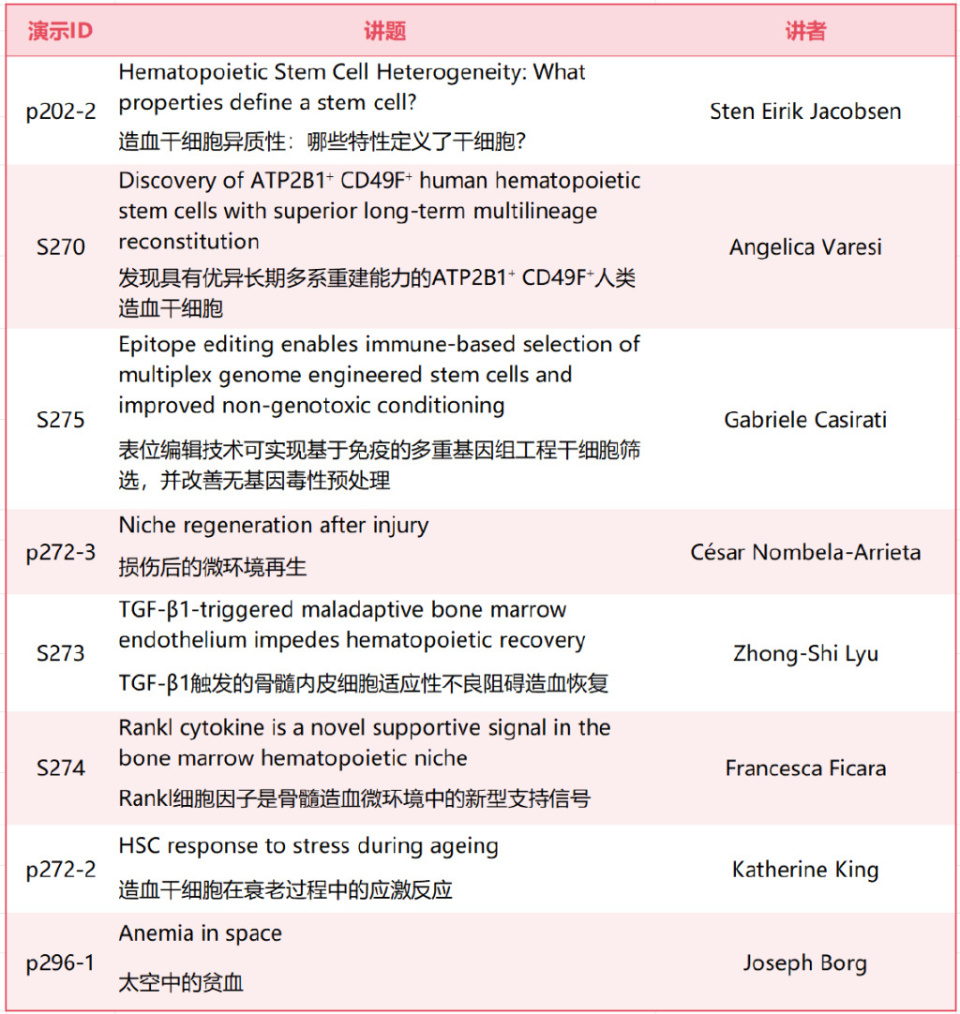
1. Jacobsen SE. Hematopoietic Stem Cell Heterogeneity: What properties define a stem cell? Oral presentation P202-2 at EHA2025.
2. Varesi A. Discovery of ATP2B1+ CD49F+ human hematopoietic stem cells with superior long-term multilineage reconstitution. Oral presentation S270 at EHA2025.
3. Casirati G. Epitope editing enables immune-based selection of multiplex genome engineered stem cells and improved non-genotoxic conditioning. Oral Abstract S275 at EHA2025.
4. Nombela-Arrieta C. Niche regeneration after injury. Oral presentation p272-3 at EHA2025.
5. Lyu ZS. TGF-β1-triggered maladaptive bone marrow endothelium impedes hematopoietic recovery. Oral presentation S273 at EHA2025.
6. Ficara F. RANKL cytokine is a novel supportive signal in the bone marrow hematopoietic niche. Oral abstract S274 at EHA2025.
7. King K. HSC response to stress during ageing. Oral presentation p272-2 at EHA2025.
8. Borg J. Anemia in space. Oral presentation p296-1 at EHA2025.