复发/难治中枢神经系统淋巴瘤(R/R CNSL)的生存预后差,其预后受多种因素影响而存在着显著差异。对于一部分再次诱导治疗达到缓解的患者,指南推荐的标准治疗是进行自体造血干细胞移植(ASCT)巩固治疗。近年来,随着嵌合抗原受体T(CAR-T)细胞治疗用于R/R CNSL的研究显示其疗效好且不良反应可控,对淋巴瘤医生提出了一个新的亟待研究的临床问题:对于化疗仍敏感、复发后再次诱导达到缓解的R/R CNSL患者,应用CAR-T细胞巩固治疗能否达到与ASCT相同的疗效?目前这样的研究相对较少。
近期,北京高博医院淋巴瘤骨髓瘤科胡凯教授团队近日在Cancer Immunology, Immunotherapy杂志发表了一篇题为“Outcomes in patients with refractory/relapsed CNS lymphoma treated in complete remission: autologous transplantation vs. CAR‑T therapy”的论文,第一作者为杨帆医生。该文章针对这一问题将团队的研究结果进行了总结,为各位专家学者在再次诱导达到缓解患者的R/R CNSL患者巩固治疗方式选择的领域提供了新的思路。
研究背景
胡凯教授谈到:复发/难治中枢神经系统淋巴瘤(R/R CNSL)的治疗很棘手,对于化疗敏感仍有机会达到完全缓解的患者,巩固治疗的方式选择非常重要。CAR-T细胞治疗的巩固能否达到自体造血干细胞移植(ASCT)的缓解深度,进而让这部分患者后期降低复发率达到长期生存的目的,是临床医生在实践中会遇到的很实际的问题。为此,我们团队的杨帆医生总结分析了60例经过化疗再次达到完全缓解的R/R CNSL 患者,其中原发性 CNSL 42例(70%),伴中枢神经系统继发受累的弥漫大B细胞淋巴瘤(DLBCL)18例(30%)。比较了患者后续行ASCT或CAR-T巩固治疗的生存期和复发率。研究排除了之前进行过ASCT的患者。
研究亮点
01、与CAR-T治疗相比, ASCT巩固可明显改善3年的PFS和累积复发率
研究显示:中位随访时间为12.1个月(范围1.28-59.9个月),与CAR-T组患者相比,达到完全缓解(CR)状态时接受 ASCT 治疗的患者具有更优的无进展生存期(PFS)[3年 PFS 80%(95%CI:48.4-93.4)vs. 64.8%(95%CI:38.9-81.9);P=0.026],且复发/进展累积发生率更低[3年复发率20%(95%CI:4.12-44.39)vs. 30.2%(95%CI:11.0-52.2);P=0.038]。原发中枢神经系统淋巴瘤(PCNSL) 患者中,ASCT 组的2年PFS显著更高[92.9%(95% CI:59.1–99.9)vs. 65.7%(95% CI:31.0–86.0);P=0.026]。 继发中枢神经系统淋巴瘤(SCNSL) 患者中, ASCT 组的2年 PFS 和OS有更高的趋势。
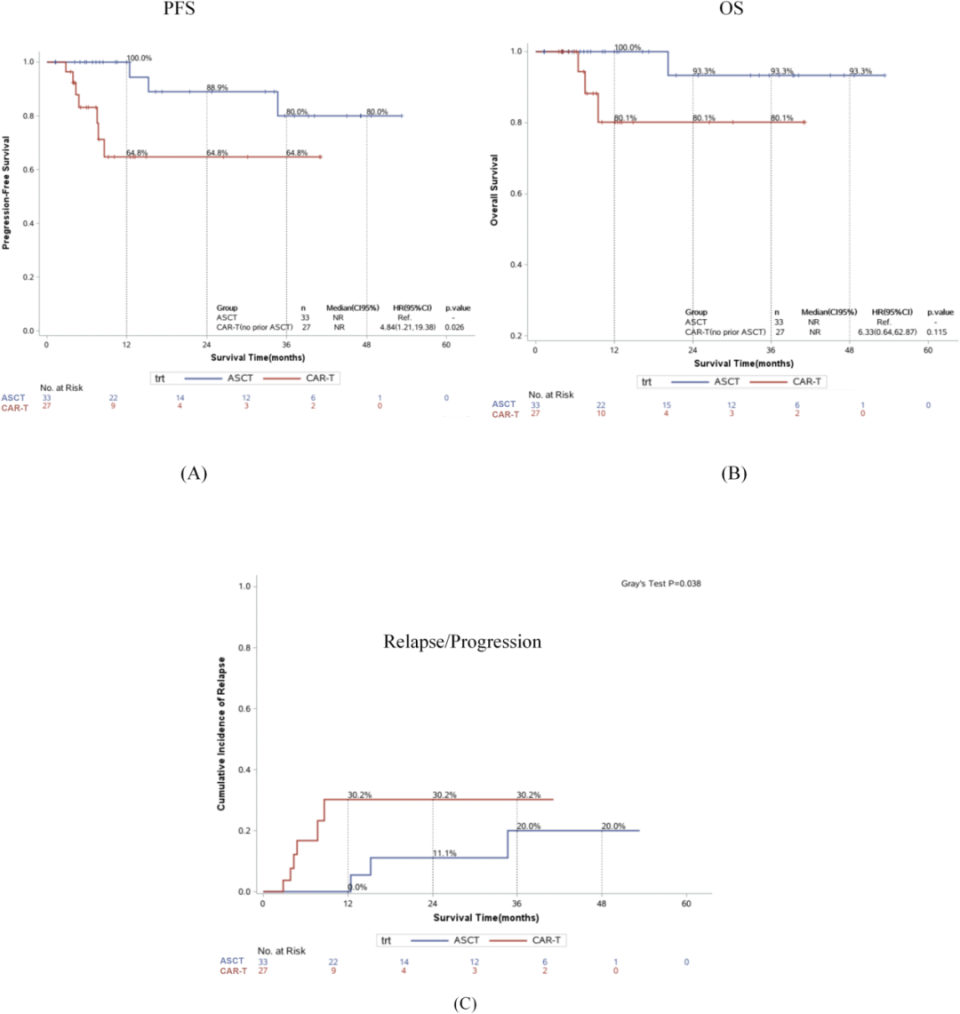
图1
02、观察到CAR-T细胞脑脊液扩增,安全性可控
输注的CAR-T细胞中位数为1.75×10⁶个细胞/kg(范围:0.16×10⁶个细胞/kg至10×10⁶个细胞/kg)。我们观察到36/37例患者输注后外周血中CAR-T细胞显著扩增(图2A)。CD19+CAR-T细胞的中位峰值数量为7465个慢病毒拷贝/ μg DNA(范围:1246–36,107个慢病毒拷贝/ μg DNA),达到峰值水平的中位时间为10天(范围:6–28天)。输注后对10例患者的脑脊液进行了评估(图2B),其中4例患者检测到CAR-T细胞。CD19+CAR-T细胞的峰值数量为2415个慢病毒拷贝/ µg DNA(范围:81–2914个慢病毒拷贝/ µg DNA)。
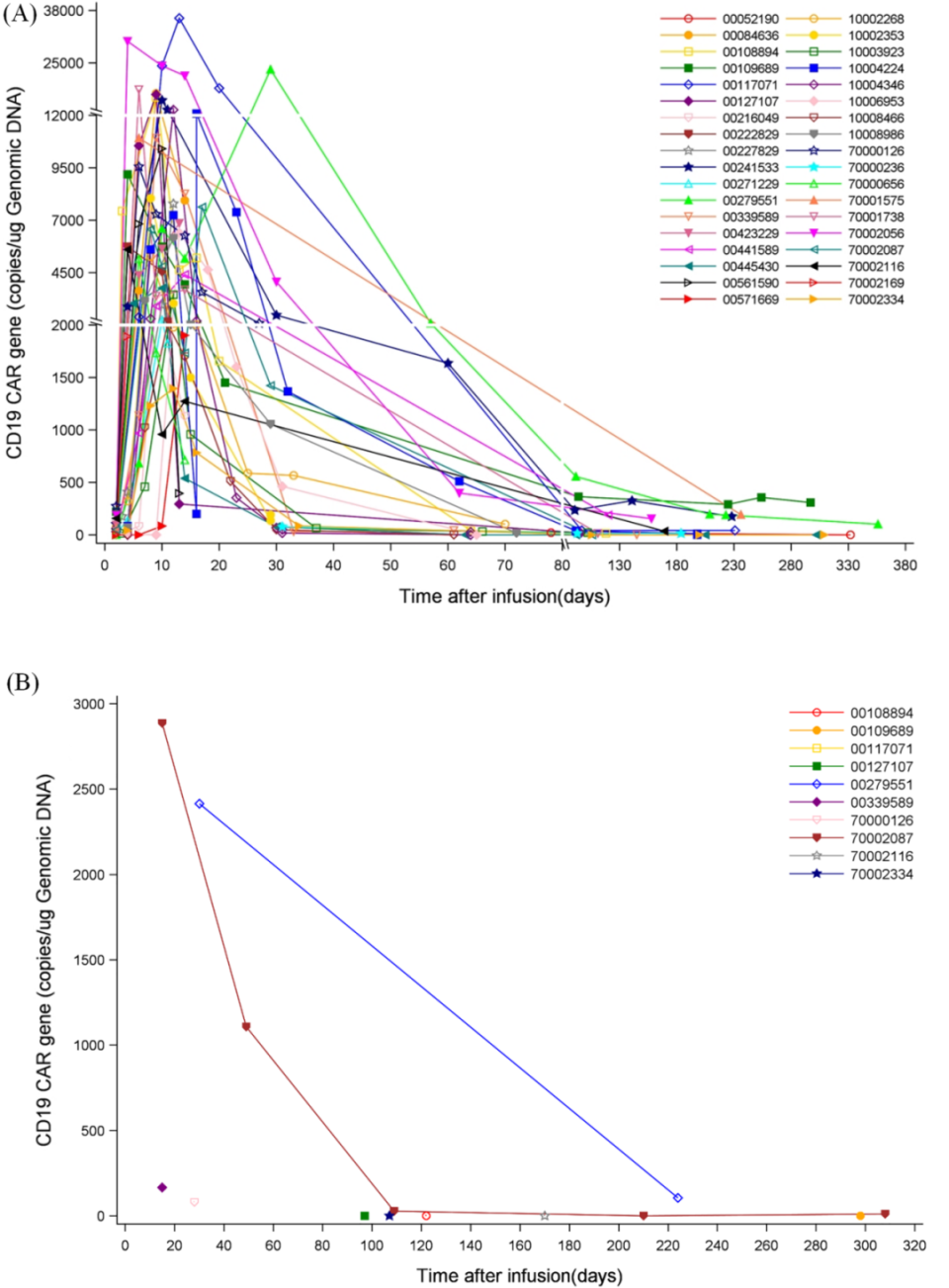
图2
最常见的不良反应为中性粒细胞减少症[57例(95%)],其次为感染[34例(56.7%)]和低丙种球蛋白血症[28例(46.7%)]。在CAR-T组中,6例患者(22.3%)出现1级CRS,3例(11.1%)发生1-2级ICANS。安全性可控。
03、观察到ASCT及CAR-T的巩固治疗对于TP53或MYD88/CD79b突变的患者均有一定的控制趋势
在获得CR后接受 ASCT(n=7)或CAR-T治疗(n=11)的突变患者预后分析显示, ASCT 组中所有可检测到Tp53或MYD88/CD79b突变的患者均存活。其中Tp53突变患者中1例出现疾病进展,2例达到CR;而MYD88/CD79b突变患者仅1例进展,其余9例均达CR。CAR-T组中5例Tp53突变患者全部存活,1例进展,4例维持CR;16例MYD88/CD79b突变患者中1例因疾病进展死亡,2例肿瘤存活,13例维持CR。仍需扩大样本量进一步研究巩固治疗对于的基因突变的控制趋势。
我们中心的初步研究显示:ASCT 巩固治疗仍是对二线化疗敏感且达到完全缓解(CR)的R/R CNSL 患者的首选巩固治疗策略。对于达到CR但不符合 ASCT 条件的R/R CNSL 患者,CAR-T疗法作为一种巩固治疗方案可能具有潜在可行性。
总结及展望
胡凯教授指出,北京高博医院淋巴瘤骨髓瘤科近年来积累了丰富的中枢神经系统淋巴瘤CAR-T治疗经验,随着真实世界中CAR-T治疗的病例逐步增多,面临的临床问题更加复杂。选择合适的CAR-T治疗时机,探索个性化、精细化、全程化的管理,仍然是血液肿瘤领域未来主要的临床任务。未来可以结合临床、病理、分子、影像等整合诊断技术来帮助我们更早了解哪些对常规治疗无效的R/R CNSL患者可从精准化CAR-T治疗中获益,并且可以通过监测ctDNA等方式提早发现复发倾向,抢先治疗,从而延长患者生存。
专家简介

胡凯 教授
北京高博医院
主任医师,医学博士,北京高博医院淋巴瘤骨髓瘤科主任
从事血液肿瘤科工作20余年,2019至今任淋巴瘤骨髓瘤科科主任,专业方向为血液系统恶性肿瘤如白血病、淋巴瘤及多发性骨髓瘤的标准化诊治,主攻免疫治疗(CAR-T细胞治疗,抗体及靶向免疫治疗等);擅长综合规范化治疗、细胞免疫治疗、抗体类药物及分子靶向治疗、自体/异体造血干细胞移植及生物治疗的综合应用,以及自体/异体造血干细胞移植治疗血液系统恶性肿瘤及移植后合并症的诊治,已有千例以上免疫治疗淋巴瘤及骨髓瘤的临床经验;其中,CAR-T细胞治疗复发/难治大B细胞淋巴瘤、T细胞淋巴瘤、中枢神经系统淋巴瘤、多发性骨髓瘤及CD19 CAR-T治疗失败后的探索性研究发表SCI论文40余篇,累计影响因子100分左右;其中,序贯二次CAR-T治疗、CAR-T联合ASCT治疗及异体CART结合异体造血干细胞移植治疗淋巴瘤及骨髓瘤更为国际领先模式,得到国内外学者广泛关注及认可。深耕临床的同时,作为主要研究者开展临床试验(IND及IIT)近40项,共参研100余项。团队的各项研究成果多次在ASH(美国血液学年会)、EHA(欧洲血液学年会)、EBMT做了大会发言,并代表国内顶尖学者成为EBMT成员。拥有科研专利一项(专利号:201420394032X),参编参译著作7本,主编3本。在多个学术团体任职。
学术任职:
中国老年学学会老年肿瘤专业委员会委员;
中国抗癌协会血液肿瘤专业委员会第一届中国T细胞淋巴瘤工作组委员;
中国健康管理协会健康科普专业委员会委员;
中国医药教育协会造血干细胞移植及细胞治疗专业委员会委员;
北京建促会血液肿瘤精准诊疗专家委员会主任委员;
北京医学会市级“枢纽型”社会组织专家委员;
北京围手术期医学研究会血液专业委员会委员;
北京肿瘤协会临床研究专业委员会委员;
北京市医学会血液委员会青年委员

杨帆
北京高博医院
副主任医师,医学硕士,北京高博医院淋巴瘤骨髓瘤科副主任
从事血液科工作近20年,专业方向为复发难治白血病、淋巴瘤、多发性骨髓瘤的CAR-T治疗及造血干细胞移植治疗,及移植后合并症的诊治。近年多次在ASH(美国血液学年会)、EBMT(欧洲移植学会)、EHA(欧洲血液学年会)、APBMT(亚太地区血液学年后)、淋巴瘤骨髓瘤免疫与靶向治疗国际高峰论坛、中国女医师协会血液学专委会分会大会均做了大会发言,代表团队在国际大会做壁报展示20余次,得到国内外广泛关注及认可。参写SCI文章20余篇,任新版《淋巴瘤靶向及免疫治疗手册》副主编。对难治/复发白血病、淋巴瘤患者的治疗有独到见解,对处理CAR-T细胞免疫治疗、移植后急、慢性移植物抗宿主病、VOD、TMA、PTLD、感染、复发、CART后CRS及ICANS等并发症有丰富经验。
学术任职:
中国女医师协会第一届靶向专业委员会常委
北京建促会血液肿瘤精准诊疗专家委员会秘书长
北京癌症防治学会淋巴瘤免疫治疗专业委员会委员;
北京癌症防治学会血液病工作委员会红细胞疾病专委会委员
中国女医师协会第一届血液专业委员会委员
中国女医师协会血液淋巴专委会委员
中国女医师协会血液学专委会白血病学组委员
中国女医师协会血液学专委会多发性骨髓瘤及相关疾病专业学组委员
高博医疗集团成人淋巴瘤(秘书)、免疫治疗、造血干细胞移植专委会委员