编者按:成人B细胞前体急性淋巴细胞白血病(B-cell precursor acute lymphoblastic leukemia, BCP-ALL)的治疗在过去十年间经历了深刻的变革。传统化疗虽取得了一定进展,但对于成人患者,尤其是老年或复发/难治性(R/R)患者,预后仍不理想。免疫疗法的出现,通过调动患者自身的免疫系统来精准靶向并清除白血病细胞,为这一领域带来了革命性的突破。近期Blood Advances发表的一篇综述文章系统梳理了免疫疗法在成人BCP-ALL前线治疗中的应用,聚焦于其作用机制、最佳使用时机、获益人群以及当前面临的挑战与未来方向。

免疫疗法的核心模式与作用机制
目前,应用于BCP-ALL的免疫疗法主要分为三大类:双特异性T细胞衔接器(BiTE)、抗体药物偶联物(ADC)和嵌合抗原受体T细胞(CAR-T)疗法。
1、靶向CD19的BiTE:贝林妥欧单抗
贝林妥欧单抗是一种典型的BiTE,其设计能同时结合B细胞表面的CD19抗原和T细胞表面的CD3受体,从而在T细胞和白血病细胞之间搭建起一座“桥梁”,促进细胞毒性突触的形成,引导T细胞杀伤白血病细胞。这一机制使其不依赖于主要组织相容性复合体(MHC)的呈递,能够高效激活内源性T细胞。
其疗效在多项关键临床试验中得到验证。在复发/难治性(R/R)BCP-ALL患者中,贝林妥欧单抗相较于标准化疗显著改善了总生存期(OS)。更重要的是,其在清除微小残留病(MRD)方面表现出色。BLAST试验显示,贝林妥欧单抗能使78%的血液学完全缓解(CHR)但MRD阳性的患者转为MRD阴性。这为其从前线巩固治疗阶段介入奠定了基础。
2、靶向CD22的ADC:奥加伊妥珠单抗
奥加伊妥珠单抗(InO)是一种ADC,由靶向CD22的单克隆抗体与细胞毒性药物卡奇霉素偶联而成。当InO与CD22结合后,会被内吞入细胞,释放卡奇霉素,导致DNA损伤和细胞死亡。
在R/R BCP-ALL的INOVATE III期试验中,InO相比化疗获得了更高的完全缓解(CR)率和MRD阴性率。与贝林妥欧单抗类似,InO也被探索用于前线治疗,特别是在老年或 unfit 患者中,作为诱导治疗的一部分,以期用更低的化疗强度获得深度缓解。
3、嵌合抗原受体T细胞疗法
CAR-T疗法通过基因工程改造患者自身的T细胞,使其表达能够特异性识别肿瘤抗原(如CD19)的受体,从而实现对白血病细胞的精准、强力且持续的杀伤。Tisagenlecleucel和Brexucabtagene autoleucel等CD19靶向CAR-T产品在儿童/青年及成人R/R BCP-ALL中取得了高达81%和71%的CR率,并获得了监管批准。
CAR-T疗法的独特优势在于其潜在的“一次输注、长期有效”的特点。即使在既往接受过贝林妥欧单抗治疗失败的患者中,CAR-T疗法仍能诱导缓解。然而,其临床应用受到制造周期、毒性管理以及抗原逃逸所致复发等问题的制约。
前线治疗中的整合策略:“何时”与“如何”使用
将上述免疫疗法整合进新诊断成人BCP-ALL的前线治疗,是当前的研究热点和临床实践演变的方向。
1、费城染色体阴性(Ph⁻)BCP-ALL
对于Ph⁻BCP-ALL,贝林妥欧单抗在巩固阶段的加入已成为重要策略。E1910 III期随机试验证明,在诱导和强化化疗后,于巩固化疗中穿插4个周期的贝林妥欧单抗,能显著改善MRD阴性患者的3年OS(85% vs. 68%,图1)。这一获益在55岁以下患者中尤为明显。基于此,贝林妥欧单抗联合巩固化疗已获准用于所有年龄患者的前线治疗。
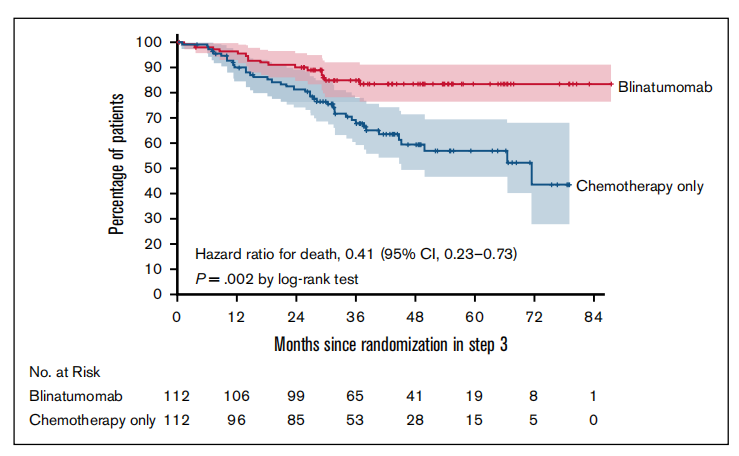 图1. 贝林妥欧单抗用于 MRD 阴性 ALL
图1. 贝林妥欧单抗用于 MRD 阴性 ALL
对于老年或unfit患者,减少或避免传统高强度化疗的“化疗减量”策略正在探索中。例如,SWOG的II期试验在≥65岁患者中使用贝林妥欧单抗进行诱导/巩固,随后接POMP方案维持,取得了可观的疗效。更激进的“无化疗”方案也在研究中,如Alliance的A041703试验,在≥60岁患者中序贯使用InO和贝林妥欧单抗,累计CR/CRi率达97%,1年OS达84%。德国GMALL的INITIAL-1试验则在>55岁患者中使用InO联合地塞米松诱导,随后进行年龄适配的化疗巩固,3年OS达73%。
2、费城染色体阳性(Ph⁺)BCP-ALL
在Ph⁺ BCP-ALL的治疗中,免疫疗法与酪氨酸激酶抑制剂(TKI)的联合展现了取代化疗的潜力。GIMEMA的D-ALBA试验使用达沙替尼联合Blinatumomab,使新诊断患者的CR率达98%,长期随访显示4年无事件生存(EFS)和OS分别达75%和81%。另一项研究将Blinatumomab与帕纳替尼联用,在24个月中位随访时,完全分子学缓解(CMR)率和MRD阴性率分别达到83%和98%。这些令人鼓舞的数据促使了多项III期随机试验的开展,旨在直接比较“TKI+免疫疗法”与“TKI+化疗”的优劣。
3、CAR-T疗法在前线的潜在角色
鉴于CAR-T在R/R和MRD阳性疾病中的卓越疗效,其在前线治疗中的应用也备受期待。一个合理的设想是,对于诱导治疗后仍为MRD阳性的患者,使用CAR-T疗法将其转为MRD阴性,从而可能免于后续强化化疗或作为异基因造血干细胞移植(allo-HCT)的桥梁。随着CAR-T制造时间缩短、毒性降低的新产品出现,这一设想将更具可行性。
关键挑战与应对策略
尽管前景光明,免疫疗法的整合仍面临多重挑战。
1、耐药与复发
抗原丢失是导致贝林妥欧单抗和CAR-T治疗失败的主要原因。研究表明,接受贝林妥欧单抗治疗后复发的患者中,约28%出现CD19阴性复发。TP53突变与CD19阴性复发风险增加相关。对于InO,CD22阴性克隆的出现、CD22的截短突变或选择性剪接是重要的耐药机制。应对策略包括开发双靶点(如CD19/CD22)CAR-T疗法,或探索其他靶点如CD20、CD123等。此外,T细胞耗竭也可能导致贝林妥欧单抗耐药,联合使用免疫检查点抑制剂(如PD-1抑制剂)正在早期试验中进行评估。
2、治疗相关毒性
不同免疫疗法的毒性谱各异。贝林妥欧单抗主要与细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)相关,但通常为低级别,且几乎无治疗相关死亡报告。InO则需重点关注肝毒性,尤其是肝窦阻塞综合征(SOS),特别是在后续接受allo-HCT的患者中风险增高。此外,InO与化疗联用时可导致严重的骨髓抑制和感染风险增加,这在年轻患者的临床试验中已观察到。CAR-T疗法的CRS和ICANS发生率和严重程度最高。因此,精准的毒性预测、预防和管理至关重要。
3、allo-HCT角色的重新定义
随着免疫疗法使更多患者获得深度分子学缓解,allo-HCT在首次完全缓解期(CR1)中的作用正被重新评估。对于通过TKI联合免疫疗法快速获得MRD阴性的Ph⁺BCP-ALL患者,可能避免在CR1期进行移植。同样,在Ph⁻患者中,allo-HCT可能更多地保留给那些具有高危遗传学特征或经免疫疗法治疗后仍无法清除MRD的患者。移植后,免疫疗法(如供者淋巴细胞输注、靶向免疫治疗)也可用于管理MRD或预防复发。
未来展望与个体化治疗
展望未来,成人BCP-ALL的治疗将更加趋向于精准和个体化。作者提出了几种可能的前线治疗框架:一是在高强度化疗(如hyper-CVAD)基础上加入InO,并用多个周期的贝林妥欧单抗替代后期化疗;二是对老年患者采用无化疗或低强度化疗联合InO和/或贝林妥欧单抗的策略;三是对年轻患者,采用InO进行诱导以获得深度缓解,随后用化疗联合贝林妥欧单抗进行巩固,并可能为MRD阳性患者预留CAR-T疗法。图2展示了一个针对青少年和年轻成人患者的可能临床试验设计框架。
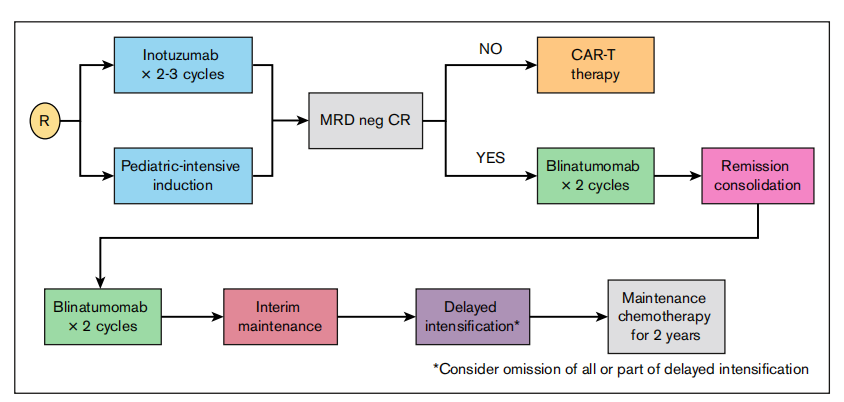 图2. 一项针对青少年和年轻成人的 BCP-ALL 试验方案
图2. 一项针对青少年和年轻成人的 BCP-ALL 试验方案
此外,联合其他靶向药物(如BCL-2抑制剂维奈克拉)、寻找预测疗效和毒性的生物标志物(如靶抗原表达水平、肿瘤微环境构成),以及优化治疗周期数(例如贝林妥欧单抗的最佳周期数仍在探索中),都是未来重要的研究方向。对于Ph⁺BCP-ALL采用无化疗方案时,还需密切关注并采取措施降低中枢神经系统复发风险。
结 论
总之,免疫疗法已从根本上改变了成人BCP-ALL的治疗格局。贝林妥欧单抗、InO和CAR-T等药物通过不同的机制,为患者提供了高效且相对特异性的治疗选择。成功整合这些疗法于前线治疗的关键在于把握最佳时机(如巩固阶段或诱导阶段)、选择合适人群(基于年龄、遗传风险、MRD状态等),并妥善管理其独特的毒性。随着对耐药机制理解的深入、新型靶点和联合策略的探索,以及个体化治疗决策工具的完善,免疫疗法有望进一步提升成人BCP-ALL的治愈率,让更多患者受益。
参考文献:
Datta S, Litzow MR. Immunotherapy in the up-front treatment of adult B-cell precursor acute lymphoblastic leukemia: when, how, who? Blood Adv. 2026 Feb 24;10(4):999-1011. doi: 10.1182/bloodadvances.2025015936. PMID: 41115238; PMCID: PMC12914415.