编者按:津门冬暖聚贤才,智启血液新未来。2026年1月9日-11日,第六届中国血液学科发展大会(CASH)在天津顺利召开。会上,中国医学科学院血液病医院(中国医学科学院血液学研究所)付荣凤教授带来“2025ASH出凝血领域研究进展汇报”专题报告,系统梳理了2025年美国血液学会(ASH)年会上原发免疫性血小板减少症(ITP)、血友病等疾病的机制研究新发现、新型治疗策略突破及重磅临床研究数据,为我国出凝血疾病诊疗的规范化与精准化发展提供了重要参考。本文特结合报告核心内容,对该领域关键进展进行深度解读。

ITP
迈向“免疫稳态重建”的精准治疗新时代
随着临床研究的持续深入,学界对ITP病理机制的认知已日益深化。ITP不再被简单界定为单纯的抗体介导性疾病,而是一种涉及B细胞、T细胞、巨噬细胞及骨髓微环境等多重免疫环节失调的系统性免疫紊乱疾病。具体而言,自身抗体通过Fc受体介导的吞噬和补体途径加速血小板破坏,同时,细胞毒性T细胞(CTL)的直接攻击和干扰素-γ等细胞因子对巨噬细胞的激活,构成了复杂的细胞免疫破坏网络。另一方面,自身抗体或炎症因子(如TNF-α)抑制巨核细胞成熟,加之调节性T细胞(Treg)功能缺陷、辅助性T细胞(Th1/Th17)比例失衡等骨髓免疫微环境异常,共同导致了血小板“生产不足”。这种多环节、多细胞参与的免疫紊乱,为靶向治疗提供了多元靶点。
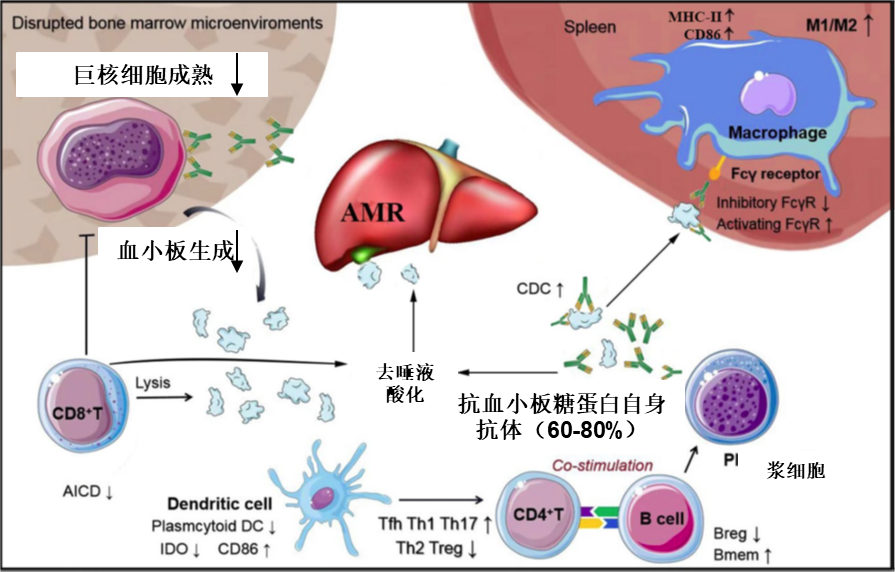 ITP发病机制
ITP发病机制
当前,国内外ITP诊疗指南已就核心治疗推荐达成共识,血小板生成素受体激动剂(TPO-RAs)仍是二线治疗的关键方案。但随着临床研究的不断推进及患者对生活质量的诉求日益提升,ITP的治疗目标已从“短期安全控制症状”迭代为“追求停药后持续缓解”的长期获益。在此背景下,针对ITP特定免疫环节的新型靶向药物不断涌现,不仅丰富了治疗选择,也为临床实现停药后持续缓解的治疗目标提供了全新路径与策略支撑。
靶向B细胞通路:Ianalumab的双重机制
BAFF信号通路是B细胞存活、活化的关键。研究发现,ITP患者血清BAFF水平升高,使其成为潜在治疗靶点。Ianalumab作为一种新型单克隆抗体,创新性地融合了“BAFF-R信号阻断”与“ADCC介导的B细胞清除”双重机制。2025 ASH公布的VAYHIT3研究数据显示,在多线治疗失败的ITP患者中,Ianalumab能实现快速、深度的B细胞耗竭,并展现出良好的疗效与耐受性。更值得关注的是其III期研究VAYHIT2的初步结果,对于一线激素治疗失败的患者,Ianalumab联合艾曲泊帕能显著延长至治疗失败的时间,持续应答率达62%,同时可改善患者疲劳感、减少出血事件,且安全性良好。这为减少甚至避免长期使用激素提供了强有力的新选择。
靶向巨噬细胞“吞噬”信号:Sovleplenib的源头干预
脾酪氨酸激酶在巨噬细胞活化和介导血小板吞噬中扮演核心角色。我国自主研发的高选择性Syk抑制剂Sovleplenib,其III期ESLIM-01研究的长期随访结果令人鼓舞。Sovleplenib治疗成人慢性ITP的总体应答率达81.0%,长期持久缓解率为61.5%,首次达到PLT≥50×10⁹/L的中位时间仅8天,且在长达3年的治疗中,出血事件发生率持续降低,胃肠道毒性等不良反应发生率较低,为既往治疗无效的患者提供了新选择。
重塑一线治疗格局:联合方案的优化探索
此外,联合治疗策略也展现出一定优势。地塞米松联合罗普司亭的Ⅲ期研究期中分析显示,该方案治疗新诊断ITP的停药6个月持续应答率(SROT)达52.9%,显著高于地塞米松单药组的30.2%,同时可减少地塞米松使用周期,降低激素相关不良反应风险。而PI3K抑制剂林普利塞、组蛋白去乙酰化酶抑制剂西达本胺等新型药物的临床研究也显示出良好前景,其中林普利塞治疗经深度预处理ITP患者的12周总体应答率达66.67%,西达本胺5mg每周两次剂量组的12周应答率达43.3%,为难治性患者提供了更多治疗选择。
血友病
步入“非因子”与“根治性”探索的广阔蓝海
血友病是因凝血因子Ⅷ(血友病A)或Ⅸ(血友病B)缺乏导致的遗传性出血性疾病,其中抑制物的产生是治疗最严峻的挑战——重型血友病A患者抑制物发生率达30%,轻/中型为5%,血友病B患者为3%。抑制物可直接中和凝血因子活性,导致替代治疗失效,显著增加出血风险与治疗负担。此外,传统凝血因子替代治疗需频繁静脉给药,患者治疗负担重,长期依从性不佳,亟需更便捷、高效的治疗方案。
2025 ASH年会公布的多项Ⅲ期研究数据,确立了非因子治疗在血友病中的核心地位。马塔西单抗作为抗组织因子途径抑制物(TFPI)单克隆抗体,已获批用于12岁及以上血友病A/B患者的预防治疗。Ⅲ期BASIS试验结果显示,对于伴抑制物的血友病患者,马塔西单抗每周皮下注射可使年化出血率(ABR)从观察期的19.78降至1.39,降幅达93%,且安全性良好,无血栓栓塞事件发生。针对青少年患者的亚组分析显示,马塔西单抗可将ABR从常规因子替代治疗的3.36降至2.98,同时显著减少因子消耗,患者依从性达80%以上,为青少年患者提供了更适配生长发育需求的治疗选择。
新型FVIII模拟物Mim8的Ⅲ期FRONTIER2研究52周数据进一步验证了其长期疗效与安全性。Mim8采用皮下注射给药,频率可灵活调整为每周一次或每月一次,伴或不伴抑制物的血友病A患者治疗后中位ABR均为0,86%-91%的既往按需治疗患者实现52周无治疗性出血,且治疗负担显著降低,体能功能改善,关节疼痛减轻,88%-98%的患者明确偏好该治疗方案。
再平衡治疗理念的代表药物Fitusiran,通过肝靶向siRNA下调抗凝血酶(AT)表达,恢复凝血酶生成,不依赖FVIII/FIX活性。Ⅲ期研究及长期随访数据显示,Fitusiran可使血友病A/B患者(伴或不伴抑制物)的ABR降低70%-90%,长期治疗维持中位ABR约0.7-0.9,且在优化剂量策略后,安全性有所优化,无新增血栓事件,为传统治疗效果不佳的患者提供了全新治疗路径。
值得关注的是,基因治疗作为血友病的潜在治愈性方案,在2025 ASH年会上展现出重要进展。中国团队开展的低剂量AAV8-hFVIII基因治疗研究显示,对于中重度血友病A患者,2×10¹²vg/kg剂量组可实现长期FVIII表达(中位约15%-20%),ABR降低>95%,且肝酶升高更少、激素用量更低,安全性良好;4×10¹²vg/kg剂量组的FVIII活性维持在48.1%,ABR降低97.5%,为不同病情患者提供了剂量选择依据。
在抑制物根治领域,CAAR-T细胞治疗展现出突破性潜力。针对FVIII抑制物产生的致病性B细胞,研究者构建了靶向FVIIIC1或A2表位的CAAR-T细胞,体外实验显示C1-CAAR-T与A2-CAAR-T杀伤效能相当,而在动物模型中,C1+A2组合CAAR-T策略可更有效清除抑制物产生细胞,显著降低循环FVIII抑制物水平,且未观察到明显安全性问题,为血友病A抑制物的根治性治疗提供了全新思路。此外,AI驱动的抑制肽设计与CTLA4-Ig(阿巴西普)预防性用药等策略,有望突破AAV中和抗体这一基因治疗的主要障碍,为基因治疗的广泛应用奠定基础。
总结
在ITP领域,免疫失衡机制的深化认知推动了多元靶向治疗发展,联合治疗与新型小分子药物让“停药后持续缓解”成为临床目标;在血友病领域,非因子治疗凭借便捷性与强效性成为主流,基因治疗与CAAR-T技术则让“治愈”愿景逐步照进现实。展望未来,随着精准医疗技术的持续迭代与创新药物的不断涌现,出凝血疾病治疗将持续向着“精准化、长效化、治愈化”迈进。期待在“智领未来”的学科发展理念引领下,我国出凝血领域能产出更多原创性成果,让前沿技术更快惠及患者,为血液学科的高质量发展注入不竭动力。
专家简介

付荣凤 教授
中国医学科学院血液病医院(中国医学科学院血液学研究所)血栓止血诊疗中心
副主任医师 硕士生导师
中国女医师协会靶向专业委员会血小板病学组 副组长
天津市整合医学学会血液病综合诊疗专业委员会委员
天津市整合医学学会干细胞与转化医学专业委员会委员
北京癌症防治学会专业委员会委员
主持及参与国家级及省部级课题多项
在国际及国内多个知名期刊发表文章多篇。